С каким типом рака коррелирует?
Рак кишечника является третьей по частоте причиной смерти в Соединенных Штатах, как и во всем мире (41 192). Связь употребления в пищу красного мяса с раком кишечника является доказанной. Менее убедительны данные касательно связи употребления красного мяса с риском развития рака молочной железы, поджелудочной железы, легких, пищевода, желудка, печени, желудка, мочевого пузыря и простаты, а также неходжкинской лимфомы и миеломы (3-40, 45,176,177,187-190,193,197-204,207).
Виды красного мяса
По данным ВОЗ, «красным мясом называется мясо млекопитающих животных, а именно: говядина, телятина, свинина, баранина, ягнятина, конина, козлятина» (43).
«Обработанным называется мясо, которое прошло процесс соления, копчения, ферментирования, вяления и др. для улучшения вкуса или увеличения срока хранения». (43).
Основное отличие состоит в том, что переработанное красное мясо проходит больше этапов обработки, чем просто красное мясо.
Красное мясо и классификация рисков рака
ВОЗ классифицирует переработанное красное мясо как канцероген группы 1, а красное мясо как канцероген группы 2А (43 179 181 191).
Вещество из группы 1 определяется как «канцерогенный для человека», в то время как из группы 2А «может вызывать рак» (43,179,181,191).
Важно отметить, что МАИР (Международное агентство по изучению рака) относит продукт к группе 1 по такому принципу:
«Вещество может быть помещено в данную группу, когда имеется не достаточно доказательств канцерогенности его у людей, но имеется достаточно доказательств его канцерогенности у экспериментальных животных и убедительные доказательства у людей, подвергшихся его воздействию». (215) ,
Отнесение продукта к группе 2А:
«Вещество может быть отнесено к данной группе, когда нет достаточных доказательств канцерогенности его у людей и достаточных доказательств канцерогенности у экспериментальных животных, а также убедительных доказательств того, что механизмы канцерогенеза у людей и животных совпадают. В исключительных случаях вещество может быть отнесено к этой категории на основании ограниченных доказательств его канцерогенности у людей ». (215).
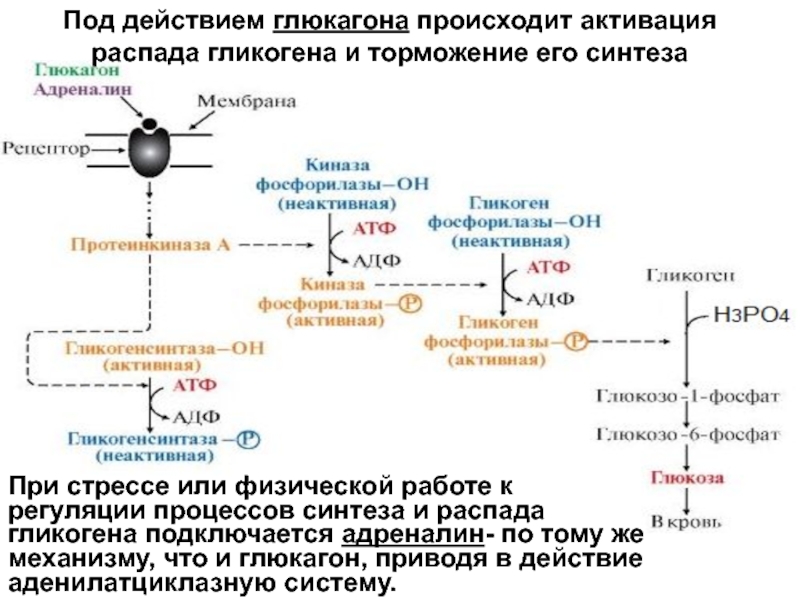
Как развивается резистентность к инсулину
Когда в организм каждый день поступает избыток глюкозы, клетки мышц и печени перенасыщаются и не могут больше поглощать и хранить глюкозу. Однако постоянное поступление глюкозы в кровь из пищи с высоким содержанием углеводов требует, чтобы глюкоза использовалась. Поскольку этого не происходит, уровень глюкозы в крови не уменьшается и постепенно растет.
Поджелудочная железа выделяет больше инсулина, чтобы сигнализировать клеткам, что уровень глюкозы в крови слишком высок, и что им нужно поглощать больше глюкозы. Клетки не могут поглощать глюкозу, они переполнены и сопротивляются ее проникновению.
Поджелудочная железа переходит в усиленный режим работы, выделяя еще больше инсулина, пытаясь преодолеть клеточное сопротивление и заставить глюкозу проникать в клетки. Развивается гиперинсулинемия, компенсирующая высокий уровень глюкозы. Некоторые эндокринологи справедливо утверждают, что лучший термин для этого ухудшающегося состояния не резистентность к инсулину, а хроническая гиперинсулинемия, так как мышцы и клетки печени на самом деле не «устойчивы» к инсулину, просто они полны и не могут реагировать, несмотря на усиление работы поджелудочной железы.
В жировой ткани увеличивается гидролиз триглицеридов, которые в ней хранятся и снижается способность поглощения липидов, циркулирующих в крови. Содержание свободных жирных кислот в плазме увеличивается, что может дополнительно ухудшить резистентность.
Как правило, клетки жировой ткани сохраняют чувствительность к инсулину при сопротивлении мышечных и клеток печени, они продолжают поглощать глюкозу и синтезировать из нее жир. Образование новой жировой ткани приводит к увеличению веса и усилению процесса резистентности к инсулину.
Определенное время компенсаторный механизм поддержания уровня глюкозы крови за счет увеличения выделения инсулина сохраняется. Но поджелудочная железа постепенно уменьшает выработку инсулина, поэтому уровень сахара также постепенно растет. Это приводит к увеличению постпрандиальной глюкозы (после приема пищи) и глюкозы в крови натощак. Отсюда нарушение толерантности к глюкозе по результатам ОГТ теста и уровня глюкозы натощак служит одними из методов определения резистентности к инсулину.
Если повышается резистентность, и прекращается работа поджелудочной железы, так как клетки со временем изнашиваются и перестают вырабатывать инсулин, может развиться диабет.
Диабет и онкологические заболевания других органов — какие органы поражаются и что повышает риски?
Диабет и онкологические заболевания других органов
Онкологические заболевания других органов при диабете развиваются как в результате системного, так и местного канцерогенеза. Ученые проводили исследования не столько в случаях рака печени и поджелудочной железы, но опухолей других органов.
Почки один из органов-мишеней, поражаемых при CD-специфической гипергликемии. Было показано, что рак почек развивается из-за общих факторов — гиперинсулинемия, ожирение, и специфических факторов, в основном гипертонии и диабетической нефропатии.
Диабетики имеют несколько более высокую заболеваемость раком мочевого пузыря. Гиперинсулинемия — не единственный частый фактор канцерогенеза в этом случае. Также могут способствовать развитию рака частые инфекции мочевыводящих путей.
Рак женской репродуктивной системы также чаще встречается у женщин с диабетом. Доказано, что у диабетиков больше шансов заболеть раком груди и слизистой оболочки матки, независимо от того, страдают они ожирением или нет. Как известно, ожирение — одна из основных причин рака груди
Но развитие этих видов рака определяют несколько механизмов, среди которых важное значение имеет действие половых гормонов.
- Гиперинсулинемия увеличивает уровень биоактивных эстрогенов в крови женщины, потому что снижается концентрация гормон-связывающего белка.
- Избыточная концентрация инсулина также стимулирует синтез андрогенов в строме яичника.
- Также является одним из механизмов развития рака репродуктивных органов женщины задержка первой менструации, особенно у девочек с диабетом типа 1. Такие женщины более склонны к бесплодию, нерегулярным менструациям и другим проблемам с фертильностью.
Результаты большинства исследований предполагают, что диабет 2-го типа связан с повышенной частотой карцином и аденом толстой кишки. Риск развития рака толстой и прямой кишки повышен и у женщин, и у мужчин.
При описании механизмов патогенеза упоминаются ряд причин:
- гиперинсулинемия;
- более медленный транзит содержимого в кишечнике;
- повышенная концентрация желчной кислоты в кале, что характерно для диабета.
Основываясь на результатах опубликованных крупных проспективных когортных исследований и исследований случай-контроль, было обнаружено, что диабетики имеют несколько более высокую вероятность развития неходжкинской лимфомы. Это объясняется нарушением работы иммунной системы из-за дисфункции нейтрофилов и изменением клеточного и гуморального иммунитета у больных диабетом.
№10: ГМО
Многие люди уже слышали термин “ГМО”. Тем не менее, далеко не все понимают, насколько на самом деле опасны генетически модифицированные организмы. Как вообще можно есть что-либо с таким неаппетитным названием? А ведь люди едят. После введения ГМО в 1996 году число людей более, чем с двумя хроническими заболеваниями подскочило с 7 до 13% всего лишь за каких-то 9 лет. Появилось гораздо больше аллергиков, детей-аутистов и пациентов с нарушениями репродуктивной функции и пищеварения.
У крыс, питающихся генетически модифицированными овощами, образуются жуткие опухоли. Гормон роста крупного рогатого скота, содержащийся в молоке, признан одним из самых опасных канцерогенов. Сторонитесь этих тихих убийц и выбирайте сертифицированные, органические продукты местного происхождения, не содержащие ГМО и производимые без применения биотехнологий. Позже вы поблагодарите себя за сознательный выбор.
Раннее выявление онкологических заболеваний
Раннее выявление и лечение онкологических заболеваний снижают связанную с ними смертность. Раннее выявление рака предполагает проведение двух комплексов мероприятий – ранней диагностики и скрининга.
Ранняя диагностика
Выявление рака на ранних стадиях повышает вероятность хорошего ответа на лечение, увеличивает шансы пациента на выживание, уменьшает тяжесть заболевания и позволяет использовать менее дорогостоящие методы лечения. Раннее выявление рака и скорейшее начало
лечения позволяют значительным образом улучшить жизнь онкологических больных.
Три составляющих успеха ранней диагностики:
- осведомленность о симптоматике различных видов рака и понимание необходимости обращения к врачу в случае возникновения признаков патологии;
- наличие возможности пройти обследование и диагностику;
- своевременное направление к специалисту для прохождения лечения.
Ранняя диагностика симптоматических форм рака актуальна в любых условиях и в отношении большинства онкологических заболеваний. Программы по борьбе с онкологическими заболеваниями должны сокращать задержки и другие факторы, препятствующие постановке диагноза,
предоставлению лечения и поддерживающего ухода.
Скрининг
Скрининг проводится с целью выявления признаков возможного наличия определенных видов рака или предраковых поражений на этапе, предшествующем развитию симптомов. При обнаружении патологических процессов в ходе скрининга пациентов направляют на дальнейшую
диагностику для подтверждения окончательного диагноза, а в случае выявления рака – на специализированное лечение.
Программы скрининга эффективны в отношении некоторых, но не всех видов рака, и, как правило, с организационной точки зрения скрининг отличается большей сложностью и ресурсоемкостью по сравнению с программами ранней диагностики, поскольку требует специального
оборудования и персонала. Наличие программ скрининга не отменяет потребности в программах ранней диагностики, поскольку они позволяют выявлять рак у людей, не отвечающих критериям прохождения скрининга по возрасту или подверженности факторами риска.
Во избежание чрезмерного количества ложноположительных результатов отбор пациентов для скрининга проводится с учетом возраста и факторов риска. Примеры методов скрининга:
- тестирование на ВПЧ (в том числе методами определения ДНК и МРНК ВПЧ) как предпочтительный способ выявления рака шейки матки; и
- маммография для выявления рака молочной железы у женщин в возрасте 50–69 лет в странах с развитыми или относительно развитыми системами здравоохранения.
В рамках программ как в области скрининга, так и в области ранней диагностики должен обеспечиваться контроль качества.
Характер проблемы
Рак — одна из ведущих причин смерти в мире, которая в 2020 г. внесла жизни почти 10 млн человек (1). В 2020 г. наиболее распространенными видами рака (с точки зрения числа новых случаев) были:
- рак молочной железы (2,26 млн случаев);
- рак легких (2,21 млн случаев);
- рак толстой и прямой кишки (1,93 млн случаев);
- рак предстательной железы (1,41 млн случаев);
- рак кожи (немеланомный) (1,20 млн случаев);
- рак желудка (1,09 млн случаев).
Наиболее распространенными причинами смерти от онкологических заболеваний в 2020 г. были:
- рак легких (1,8 млн случаев смерти);
- рак толстой и прямой кишки (916 000 случаев смерти);
- рак печени (830 000 случаев смерти);
- рак желудка (769 000 случаев смерти);
- рак молочной железы (685 000 случаев смерти).
Ежегодно рак развивается у примерно 400 000 детей. Распространенность различных видов рака варьируется в зависимости от страны. Рак шейки матки является наиболее распространенным в 23 странах.
Витамин А и рак легкого
Ретиноиды (формы витамина A или связанные с ним вещества) не имеют доказательств эффективности при лечении онкологических заболеваний у людей, кроме одного случая — промиелоцитарного лейкоза. Это заболевание обычно лечится с помощью химиотерапии и ретиноевой кислоты (природного метаболита витамина A). Что касается снижения риска развития рака благодаря ретиноидам, то бета-каротин, например, здесь плохой помощник. Если принимать его дополнительно, у курильщиков несколько повышается риск развития рака легкого.
В то же время, одно исследование, проведенное в 2015 году, показало, что витамин A может помочь витамину D в профилактике рака легких у курильщиков.
В целом результаты исследований, посвященных влиянию приема витамина A и ретиноидов на риск развития рака, неоднозначны. В некоторых экспериментах (правда, они были проведены не на людях, а на клеточных линиях и животных) было показано, что эти вещества подавляют развитие рака кожи, молочной железы, полости рта, легких, печени, желудочно-кишечного тракта, предстательной железы и мочевого пузыря. В других исследованиях ученые обнаружили, что антиоксидантные пищевые добавки, включая бета-каротин, не оказывают защитного эффекта и даже могут повысить смертность среди онкологических больных. Кроме того, в высоких дозах витамин A и ретиноиды токсичны.
Можно ли обнаружить рак легкого на ранней стадии?
Обычно симптомы рака легкого не появляются до тех пор, пока опухоль не становится распространенной. Однако в некоторых случаях рак легкого выявляется на ранней стадии, но он обнаруживается случайно при обследовании по поводу других заболеваний. Например, опухоль может быть обнаружена во время рентгенографии или компьютерной томографии грудной клетки, бронхоскопии (осмотра бронхов изнутри с помощью специального устройства — бронхоскопа) или цитологического исследования мокроты, выполненных по поводу других причин у больных с заболеваниями сердца, воспалением легких и пр.
СКРИНИНГ РАКА ЛЕГКОГО
Скрининг — это использование методов обследования с целью выявления заболевания у людей, у которых отсутствуют признаки болезни. Например, микроскопическое исследование мазка с шейки матки применяется для ранней диагностики рака шейки матки.
В связи с тем, что рак легкого обычно уже выходит за пределы легких еще до появления симптомов заболевания, эффективный скрининг с целью ранней диагностики мог бы спасти многие жизни.
Значение рентгенограмм и микроскопического исследования мокроты с целью выявления раковых клеток изучалось в течение многих лет. Результаты исследований показали, что эти методы не позволяют обнаружить многие случаи рака легкого на ранних стадиях и не увеличивают шансов на излечение. Поэтому скрининг рака легкого не является рутинной (обычной) практикой для населения и даже для лиц с повышенным риском, например, для курильщиков.
Недавно появился новый рентгенологический метод — спиральная низкодозная компьютерная томография, позволяющая выявлять рак легкого на ранних стадиях среди курильщиков. Однако еще не доказано, что данный метод даст возможность снизить вероятность смерти от рака легкого.
Люди, которые курят в настоящее время, должны осознавать, что наилучший способ избежать смерти от рака легкого — это прекратить курение. Выявление изменений в ДНК бронхиальных клеток, возможно, поможет в ранней диагностике рака легкого, однако значение таких исследований еще не доказано.
Люди, которые курили ранее или продолжают курить в настоящее время, а также те, которые находились под воздействием табачного дыма или работали с материалами, повышающими риск развития рака легкого, имеют повышенный риск рака легкого.
Начало дискуссии
В октябре 2015 года Всемирная организация здравоохранения (ВОЗ) опубликовала доклад о том, что употребление переработанного и необработанного красного мяса является причиной развития рака. (3 179 193).
Однако существует ли на самом деле причинно-следственная связь между употреблением в пищу красного мяса и раком? Каким образом употребление в пищу красного мяса может привести к раку? Что мы можем сделать, чтобы снизить потенциальный риск развития рака от употребления красного мяса, при этом, не отказываясь от него совсем? Вот некоторые из вопросов, на которые даны ответы в данной статье.
Но сначала, вот некоторые из основных выводов:
• Если вы ведете здоровый образ жизни, то умеренное потребление красного мяса не принесет вреда.
• Употребление в пищу больших количеств красного мяса вредно (особенно это касается переработанного красного мяса).
• Употребление в пищу красного мяса положительно коррелирует с раком (главным образом, с раком кишечника). Употребление красного мяса может привести к заболеванию раком, однако исследования не могут установить причинно-следственную связь, учитывая другие возможные факторы и отсутствие клинических испытаний.
• Переработанное красное мясо и риск развития рака находятся в более тесной корреляции, чем необработанное красное мясо.
• Некоторые органы власти рекомендуют употреблять «не более одной-двух порций переработанного мяса в месяц и не более одной-двух порций необработанного мяса в неделю» (1); другие предлагают <300 грамм красного и переработанного мяса в неделю (187). The World Cancer Research Fund рекомендует употреблять <500 грамм красного мяса в неделю, и очень малые количества или же совсем не употреблять переработанное красное мясо (197). Нет достаточных доказательств для окончательного определения безопасного уровня потребления.
• Потребление красного мяса может привести к раку, но вы можете снизить риски.
• Риск заболеть раком из-за употребления в пищу красного мяса относителен, так как мы можем контролировать его количество в своем рационе. Также, потребление красного мяса, безусловно, не является основным фактором, влияющим на риск развития рака (2).
• Потребление красного мяса может быть полезно, поэтому, несмотря на связь с раком, его периодическое потребление может положительно влиять на здоровье.
Как это может использоваться в борьбе с раком?
Это открытие позволяет по-новому взглянуть на терапию рака. Если норадреналин действительно с помощью сосудисто-метаболического «переключателя» стимулирует образование новых кровеносных сосудов, то терапия бета-блокаторами может обладать свойствами, препятствующими росту опухолевых клеток. Это предположение может быть проверено в клинических исследованиях в самое ближайшее время, т.к. бета-блокаторы уже много лет используются в качестве препаратов для снижения артериального давления. По мнению Френетте, перспективным могло бы быть сочетание бета-блокаторов и блокаторов сосудистого роста.
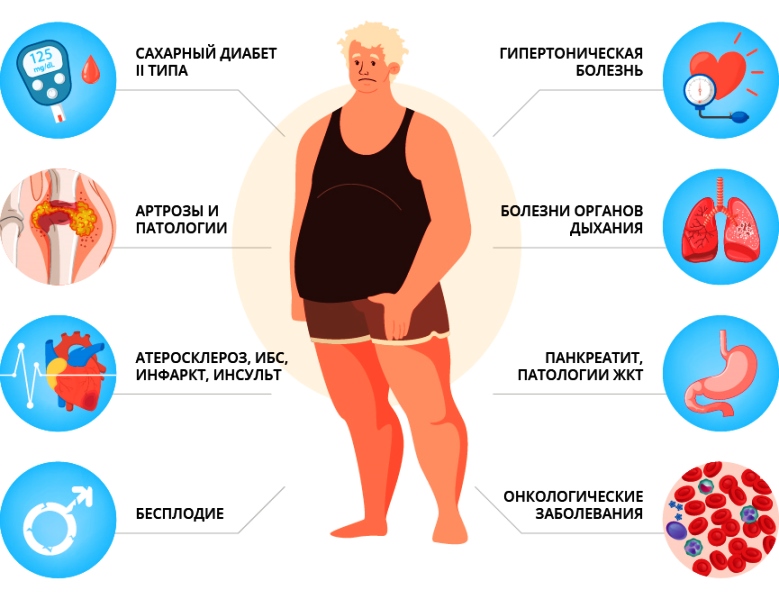
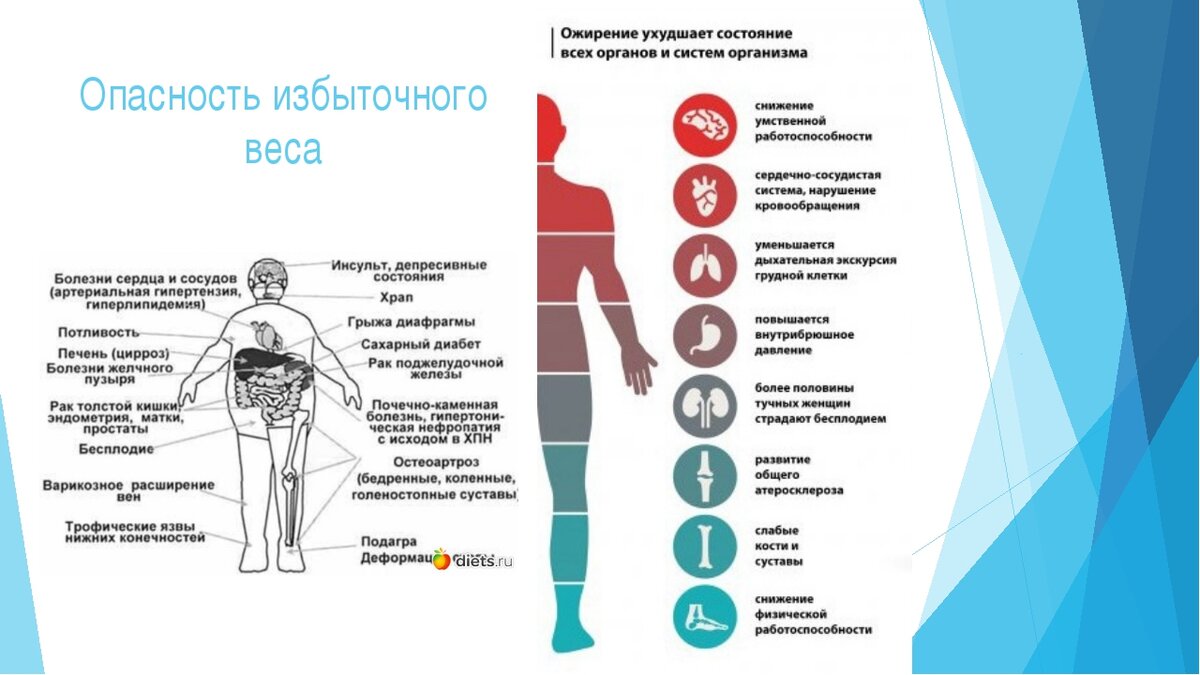
Риски развития онкологии у больных с сахарным диабетом
Риски развития онкологии
Согласно данным, предоставляемых онкологами, диабет увеличивает риск поражения печени, поджелудочной железы, толстой кишки, почек, мочевого пузыря, слизистой оболочки матки, груди и развития неходжкинской лимфомы.
Есть два типа механизмов, которые способствуют развитию злокачественных новообразований при диабете.
- Первый тип — это общие механизмы, которые способствуют онкологическим процессам во многих органах. Например, гипергликемия, гиперинсулинемия, активность препаратов, используемых при лечении сахарного диабета, поскольку они влияют на все ткани.
- Второй тип — определенные механизмы, влияющие на канцерогенез только в одном из органов.
Из-за хронического течения без выраженных симптомов диабет часто длительное время не диагностируют. Согласно эпидемиологическому исследованию, проведенному в США, у 3-5% взрослых диабет не выявлен. Доказано, что диабет является одним из факторов, повышающих риск развития злокачественных новообразований — онкологические заболевания однозначно чаще встречаются среди людей с CD
Витамин С и колоректальный рак
Витамин C очень популярен у сторонников ортомолекулярной медицины. Как и другие витамины, он не доказал свою эффективность при лечении рака, однако, по некоторым данным, может улучшать качество жизни онкологических больных. Внутривенное введение витамина C пациенткам с раком молочной железы и раком яичников улучшало их общее состояние на фоне химиотерапии или лучевой терапии. То же происходило в случаях, когда рак уже не поддавался лечению (в этой ситуации применялись высокие дозы витамина в таблетках).
А вот при лечении миелоидного лейкоза, рефрактерного колоректального рака с метастазами, меланомы с метастазами химиопрепараты в сочетании с витамином C давали серьезные побочные эффекты и ухудшали течение болезни. Также есть серьезные основания полагать, что витамин C в драже и таблетках может взаимодействовать с бортезомибом и снижать его эффективность. Кроме того, высокие дозы витамина C не следует применять людям с болезнями почек: это может привести к мочекаменной болезни или почечной недостаточности.
Вообще, впервые о витамине C как о веществе, способном уничтожать раковые клетки, начали говорить в 70-х годах прошлого столетия. И действительно, результаты первых исследований на эту тему оказались весьма обнадеживающими. Но проведенные впоследствии крупные рандомизированные исследования не показали пользы аскорбиновой кислоты для онкологических больных. В настоящее время нет ни одной серьезной крупной работы, которая бы это подтвердила.
Тем не менее, недавно у ученых вновь проснулся интерес к витамину C как к противоопухолевому средству. Во многом этому способствовала работа исследователей из Университета штата Айова (Iowa State University), опубликованная в начале 2017 года. Авторы указывают, что витамин может атаковать раковые клетки, только если он присутствует в крови в высокой концентрации, которой сложно достичь при его пероральном (то есть путем проглатывания) приеме. Если вводить аскорбиновую кислоту в обход кишечника — внутривенно, — то ее концентрация в крови будет в 100–500 раз выше. Витамин C расщепляется в организме с образованием перекиси водорода, которая повреждает ткани, ДНК. В опухолевых клетках низкая активность фермента каталазы, поэтому они не могут эффективно расщеплять перекись и страдают сильнее, чем нормальные.
Результаты этой работы нельзя воспринимать как призыв срочно принимать витамин C в убойных дозах или вводить его внутривенно. Повторимся: пока нет ни одного реального достоверного доказательства того, что это помогает в профилактике или лечении рака. К тому же, высокие дозы аскорбинки — 2000 мг в день и более — могут привести к таким побочным эффектам, как головные боли, диарея, изжога, тошнота. При длительном приеме у некоторых людей образуются камни в почках.
Основные факты
- Рак является одной из ведущих причин смерти в мире, которая в 2020 г. унесла жизни почти 10 млн человек, или почти каждого шестого умершего.
- Наиболее распространенными видами рака являются рак молочной железы, легких, толстой и прямой кишки и предстательной железы.
- Примерно одна треть случаев смерти от рака вызвана употреблением табака, высоким индексом массы тела, употреблением алкоголя, низким уровнем потребления фруктов и овощей, а также отсутствием физической активности.
- Примерно 30% случаев рака в странах с низким уровнем дохода и уровнем дохода ниже среднего обусловлено такими вызывающими рак инфекциями, как вирус папилломы человека (ВПЧ) и гепатит.
- Многие виды рака излечимы при своевременной постановке диагноза и назначении лечения.
Рак – собирательный термин, охватывающий широкую группу заболеваний, которые могут поражать любые органы и системы организма человека. Для обозначения этой категории заболеваний используются также термины «злокачественные опухоли» и
«новообразования». Одной из характерных особенностей рака является быстрое размножение аномальных клеток, разрастающихся за пределы своих обычных границ и способных проникать в окружающие ткани, а также мигрировать в другие органы, то
есть метастазировать. Распространенные метастазы – основная причина смерти от рака.
Исходный и абсолютный риски рака при употреблении красного мяса
Приведенный выше график представляет процентное изменение риска развития рака, связанное с потреблением ~ 50 г переработанного красного мяса или ~ 100 г необработанного красного мяса в день.
Например, относительный риск рака мочевого пузыря (риск по сравнению с исходным, выраженный в виде десятичной дроби) как при употреблении необработанного, так и переработанного красного мяса составляет 1,08. Таким образом, по сравнению с исходным риском (1,0), риск рака мочевого пузыря увеличивается на 8% при потреблении ~ 100 г красного мяса или ~ 50 г переработанного красного мяса в день. Это не означает, что абсолютный риск рака увеличивается на 8%; это означает, что риск заболеть раком увеличится на 8 % от 2,4% от исходного риска рака мочевого пузыря. Таким образом, первоначальный абсолютный риск 2,4% увеличивается на 0,122% (с 2,4% до 2,592%).
Несмотря на очевидное увеличение относительного риска, абсолютный риск существенно не увеличивается после употребления 100 г красного мяса или 50 г переработанного красного мяса.
№6: Картофельные чипсы
Картофельные чипсы – это дешевый, простой и аппетитный перекус. Несмотря на это, любимые многими хрустящие, вызывающие привыкание чипсы могут оказаться смертельно опасными. Такая пища способствует набору веса, так как в ней содержится большой объем трансжиров. Избыточный натрий повышает артериальное давление. Не приносят пользы и искусственные ароматизаторы, консерванты и красители.
В некоторых партиях картофельных чипсов содержится акриламид – известный канцероген, которым напичканы сигареты. Старайтесь не покупать подобную пищу ни себе, ни детям – выбирайте соленую соломку, свежий попкорн или чипсы из запеченных яблок.
Паллиативная помощь
Паллиативная помощь – это вид терапии, направленный не на излечение, а на облегчение вызываемых раком симптомов и страданий и на улучшение качества жизни пациентов и их семей. Оказание паллиативной помощи может повысить уровень комфорта онкологических
пациентов. Актуальность этого вида медицинской помощи особенно высока там, где отмечается большая доля онкологических пациентов на поздних стадиях болезни, имеющих мало шансов на излечение.
Паллиативная помощь позволяет облегчить физические, психологические, социальные и духовные страдания больных раком на поздней стадии в более чем 90% случаев.
Для лечения боли и оказания паллиативной помощи пациентам и их семьям крайне необходимо наличие эффективных стратегий в области здравоохранения, включающих оказание помощи на уровне местных сообществ и на дому.
Для лечения умеренного/тяжелого болевого синдрома, присутствующего у более 80% онкологических пациентов на терминальной стадии болезни, настоятельно рекомендуется расширение доступа к пероральному морфину.
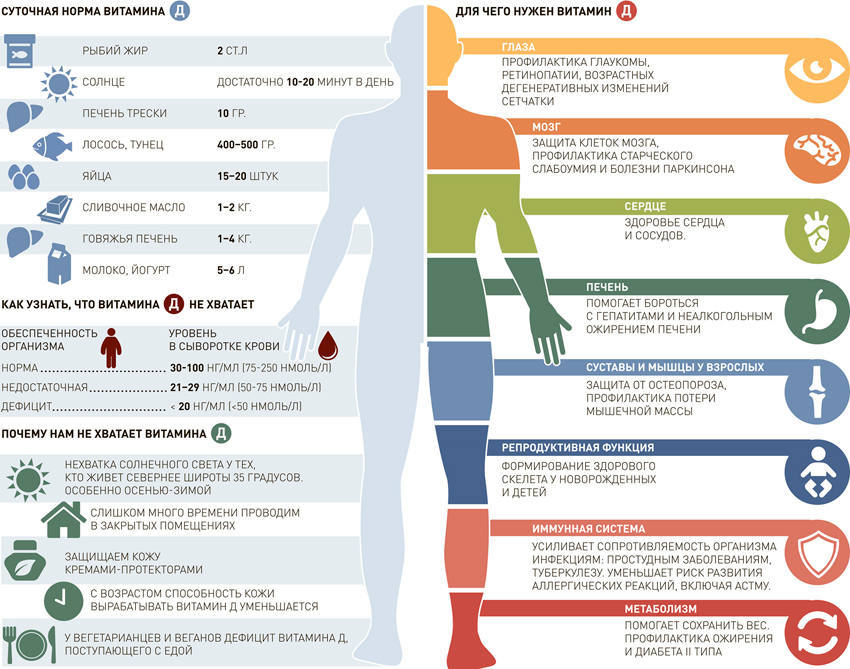
Витамин D
Это единственный витамин, который реально помогает предотвратить развитие некоторых злокачественных опухолей, и это подтверждается научными исследованиями.
Например, в 2018 году были опубликованы результаты исследования с участием 5000 женщин в возрасте 55 лет и старше. Ученые обнаружили, что у участниц с уровнем витамина D в крови 60 нг/мл и более риск развития рака молочной железы был на 80% ниже по сравнению с теми, у кого уровень витамина составил 20 нг/мл и менее. Более ранние работы подтверждают, что низкие уровни витамина D связаны с более высокими рисками развития злокачественных опухолей груди. Также была обнаружена связь между высоким содержанием витамина D в крови и более высокой выживаемостью среди женщин, у которых уже диагностировано онкологическое заболевание.
Но есть и небольшая ложка дегтя. В 2018 году исследователи из Национального онкологического института США (National Cancer Institute) провели исследование с участием 26 тысяч мужчин старше 50 лет и женщин старше 55 лет. Участников поделили на четыре группы: одним регулярно давали витамин D и плацебо, вторым — омега-3 ненасыщенные жирные кислоты, третьим — витамин и ненасыщенные кислоты, четвертым — два плацебо. После периода наблюдения оказалось, что в группах, получавших и не получавших витамин D, примерно одинаковое количество участников заболели раком и умерли от него. Ученые продолжают наблюдение, возможно, со временем разница всё-таки появится.
Известно, что низкие уровни витамина D в крови связаны с повышенным риском и других типов злокачественных опухолей, в частности, рака кишечника, мочевого пузыря.
В небольших исследованиях было установлено, что прием витамина D3 снижает скорость повышения простат-специфического антигена, являющегося признаком развития рака простаты. Однако несмотря на обнадеживающие данные в ранних исследованиях, в крупных не было замечено улучшения работы химиопрепаратов при лечении рака предстательной железы благодаря витамину D3.
Выводы
И диабет, и онкологические заболевания возникают из-за многих факторов. Эпидемиологические исследования показали статистически значимую связь между заболеваемостью СД и раком многих органов — печени, поджелудочной железы, женских репродуктивных органов, толстой кишки и т. д.
Основным фактором патогенеза рака при диабете считается гиперинсулинемия. Это состояние приводит к усилению митогенного действия инсулина, который способствует делению клеток в организме, в том числе раковых. Пациенты с CD имеют самый высокий риск развития злокачественных новообразований печени и поджелудочной железы. Рак печени развивается из-за комбинированного воздействия гиперинсулинемии и прямого повышения уровня глюкозы в крови.
Рак поджелудочной железы и диабет имеют причинно-следственную связь:
- диабет может быть вызван раком поджелудочной железы;
- рак поджелудочной железы может быть вызван диабетом.
Эти причины необходимо различать, потому что внезапное начало сахарного диабета у тучных людей среднего возраста может быть именно симптомом рака поджелудочной железы.
СД не является таким значительным фактором риска рака других органов. Например, рак мочевого пузыря развивается не только из-за гиперинсулинемии, но и из-за частых инфекций мочевыводящих путей, характерных для диабетиков.
На онкологические заболевания женской репродуктивной системы (груди, слизистой оболочки матки) влияет не только состояние диабета, но и дисбаланс половых гормонов. СД также вызывается лимфомой толстой кишки и неходжкинской лимфомой. Интересно, что мужчины с CD имеют более низкий риск развития рака простаты по сравнению с людьми без диагноза диабет.
Общая смертность увеличивается у пациентов с СД и злокачественными онкологическими заболеваниями из-за метаболических и гормональных изменений. При этом исследования показывают, что наблюдается значительное увеличение смертности от диабета и злокачественных новообразований груди, слизистой оболочки матки, толстой или прямой кишки и, в меньшей степени, от других злокачественных новообразований.
К сожалению, при лечении онкологических больных, имеющих ещё и диабет, не всегда удается назначить сильную химиотерапию, а ответ на лечение может быть неадекватным
Важно помнить, что некоторые препараты могут ухудшить состояние пациента с СД, например, глюкокортикоиды и препараты, подавляющие андрогены