Сократить повышенный уровень содержания жира в крови

Жиры, содержащиеся в крови, или липиды включают холестерин и триглицериды. Организму необходимо определенное количество холестерина, но, когда в крови слишком много жиров (гиперлипидемия), жировые отложения накапливаются в артериях, повышая риск возникновения инфарктов и инсультов. Холестерин не может растворяться в крови, поэтому ему нужны белки – носители для перемещения его по всему организму. Белки-носители называются липопротеидами. Существует два основных вида:
— Липопротеид высокой плотности (ЛВП): Когда холестерин переносится с помощью ЛВП, он называется холестерином ЛВП. Это «хороший» холестерин, понижающий риск возникновения инфаркта и инсульта.- Липопротеид низкой плотности (ЛНП): Когда холестерин переносится посредством ЛНП, он называется холестерином ЛНП. Это «плохой» холестерин, повышающий риск возникновения инфарктов и инсультов.
В некоторых семьях может постоянно наблюдаться повышенный уровень холестерина. Но наиболее часто высокий уровень содержания жира в крови вызван неправильным питанием и отсутствием физической активности. Повышенный уровень содержания жира в крови редко имеет симптомы или предупреждающие признаки. Когда уровень холестерина очень высок, у некоторых людей на коже появляются новообразования, называемые ксантомами. Для проверки уровня содержания жира в крови обращайтесь к врачу для проведения простого анализа крови.
В некоторых случаях повышенный уровень жира в крови может быть связан с невыявленным медицинским состоянием, например диабетом.
Что надо делать при повышенном уровне содержания жира в крови?
- Иметь правильный рацион питания с повышенным содержанием фруктов и овощей и пониженным содержанием животных жиров, насыщенных жиров и холестерина .
- Поддерживать нормальную массу тела.
- Сохранять физическую активность.
Если эти меры в достаточной степени не понизят уровень содержания жира в крови, врач может назначить лекарственные средства. Вы должны регулярно
их принимать, даже если не ощущаете их воздействия, а также необходимо поддерживать здоровый образ жизни.
Зоя Павлова. По материалам ВОЗ
Тем временем
Недавно американские исследователи из клиники Мауо нашли способ снизить высокое артериальное давление без лекарств. Текущие рекомендации включают, как правило, аэробные и динамические упражнения. Однако специалисты клиники выяснили, что и относительно низкоинтенсивные краткосрочные упражнения могут приносить пользу гипертоникам — упражнения нужно делать в течение всего 12 минут.
Результаты их исследования показали, что изометрические упражнения (разновидность статической нагрузки, рассчитанной не на общую выносливость, а на силу опорно-двигательного аппарата — мускулов, сухожилий, суставов) с отягощениями могут приводить к такому же эффекту снижения артериального давления, как и аэробные, а, может быть, даже к большему. Как поясняют в клинике Мауо, речь идет об упражнениях на сокращение определенной или группы мышц, которые выполняются в одном положении без движения.
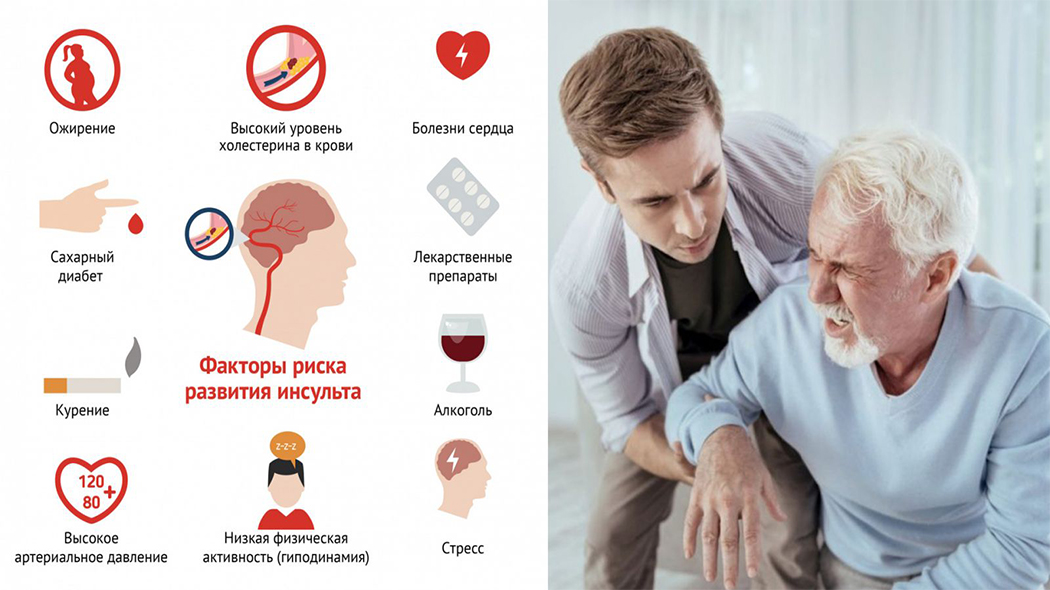
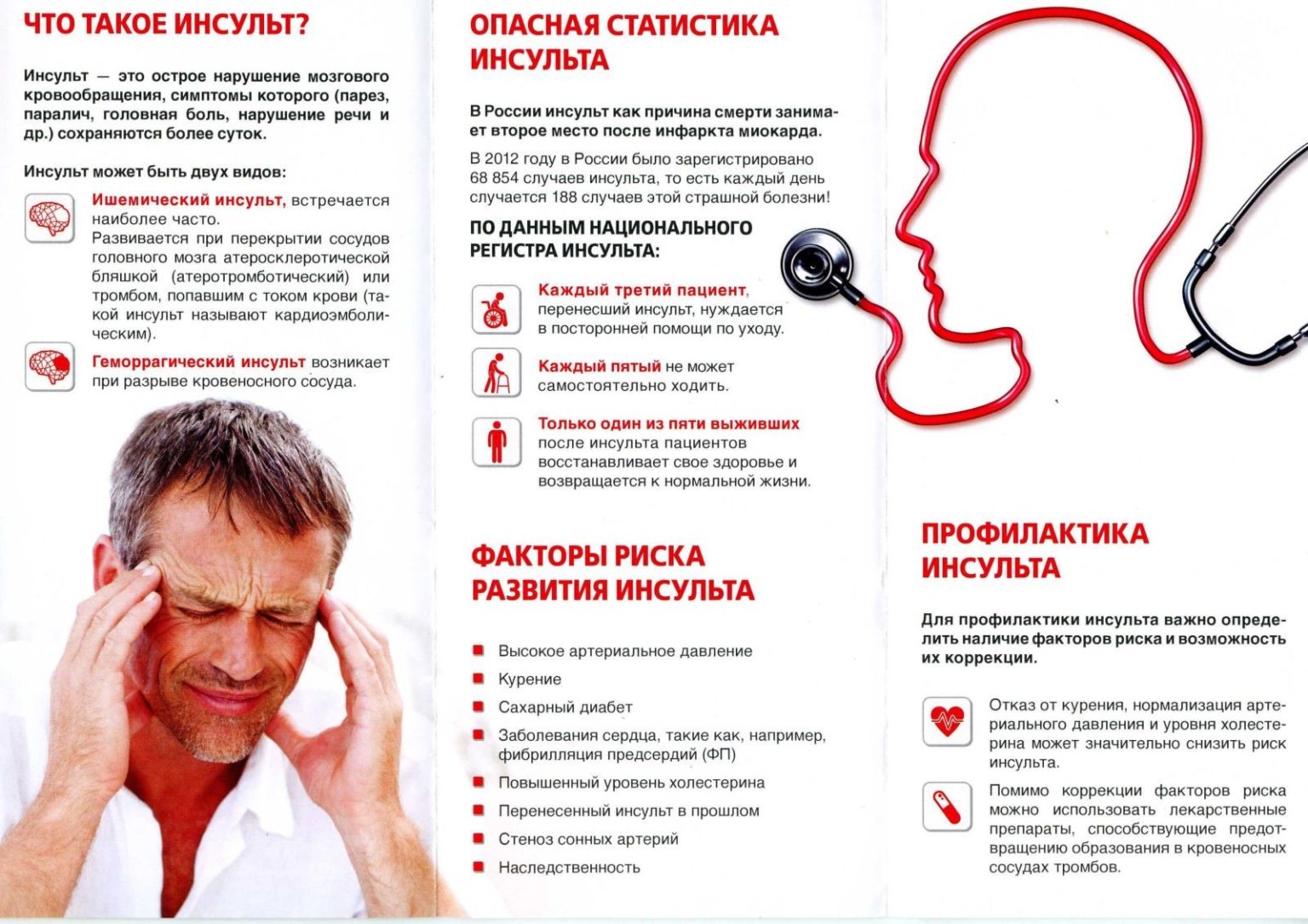
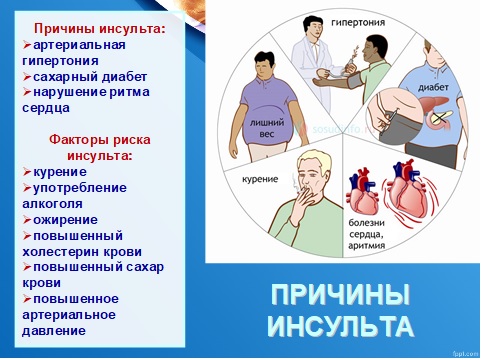
Что приближает инсульт и кому он грозит?
Главным фактором риска является возраст. Ежегодно в молодом возрасте инсульт развивается только у 1 из 90 тысяч населения, в то время как в старческом возрасте (75-84 года) он возникает у 1 из 45 человек. В 45 лет риск инсульта относительно низок в течение последующих 20 лет (возникает у одного из 30 человек), однако его вероятность к 80 годам существенно возрастает (он возникает у одного из четырёх мужчин и у одной из пяти женщин).
В целом риск развития инсульта у мужчин на 30% выше, чем у женщин. Однако это характерно только для возрастной группы населения от 45 до 64 лет. В возрасте старше 65 лет риск инсульта у мужчин и женщин практически не отличается.
К основным факторам риска инсульта также относят артериальную гипертонию , заболевания сердца , перенесённый ранее инсульт , курение , злоупотребление алкоголем , высокий уровень холестерина в крови, избыточное употребление соли. Между многими факторами существует взаимное влияние, поэтому их сочетание приводит к более значительному увеличению риска заболевания, чем простое арифметическое сложение их изолированного действия.
Временная утрата трудоспособности после сердечного приступа
Инвалидность после инфаркта миокарда устанавливается не всегда. Однако всем людям положены некоторые льготы – оплачиваемый больничный. Срок временной нетрудоспособности зависит от типа перенесенного сердечного приступа (3):
- неосложненный мелкоочаговый инфаркт – 60-70 дней. Если есть сердечная недостаточность I функционального класса (ФК) – до 80, II – до 110, III-IV – до 120;
- неосложненный крупноочаговый инфаркт – 70-90 дней, осложненный 90-120 дней.
Больничный лист сроком более 4 месяцев выдается по решению МСЭ. Если надежды на восстановление трудоспособности нет, больного признают нетрудоспособным.
Можно ли применять НПОАК при пороках сердца?
Применение НПОАК возможно только у пациентов с неклапанной ФП. При этом под «пороком сердца» следует понимать механический протез клапана сердца и средне-тяжелый или тяжелый стеноз митрального отверстия (обычно ревматической этиологии), так как именно таких пациентов исключали из всех рандомизированных клинических исследований НПОАК III фазы. Однако у пациентов с ФП нередко определяются и другие изменения клапанов сердца, которые не являются противопоказанием к назначению НПОАК (табл. 3) . К ним относятся стеноз аортального отверстия, недостаточность аортального клапана, пролапс митрального клапана, реконструктивные операции на митральном клапане, биопротезы клапанов сердца, вмешательства на аортальном клапане. Пациентов с указанными пороками сердца включали в рандомизированные контролируемые исследования, которые подтвердили эффективность и безопасность НПОАК по сравнению варфарином у таких больных .
| Состояние | Возможность назначения НПОАК |
|---|---|
| Механический протез клапана сердца | Противопоказаны |
| Средне-тяжелый или тяжелый стеноз митрального отверстия (обычно ревматической этиологии) | Противопоказаны |
| Другие легкие или средне-тяжелые пороки нативных клапанов сердца (легкие или средне-тяжелые аортальный стеноз или недостаточность, митральная недостаточность и т.д.) | Таких пациентов включали в клинические исследования |
| Тяжелый аортальный стеноз | Данные ограничены (исключали из RE-LY). Большинству пациентов проводится оперативное вмешательство. |
| Биологические протезы клапанов сердца (>3 мес после операции) | Не рекомендуются больным ревматическим митральным стенозом. Применение возможно, если протезирование выполнено по поводу митральной недостаточности или порока аортального клапана |
| Реконструктивное вмешательство на митральном клапане (>3 мес после операции) | Пациентов включали в некоторые исследования НПОАК |
| Чрескожная транслюминальная пластика аортального клапана или транскатетерная имплантация аортального клапана | Проспективные исследования не проводились. Может потребоваться комбинация с одним или двумя антитромбоцитарными препаратами |
| Гипертрофическая кардиомиопатия | Данные немногочисленны, однако применение НПОАК может быть приемлемым |
Следует отметить, что эффективность и безопасность НПОАК недостаточно изучены у пациентов с биопротезами клапанов и больных, перенесших реконструктивные вмешательства на клапанах. Большинство таких пациентов не нуждаются в длительной антикоагулянтной терапии после операции, поэтому по мнению экспертов Европейской ассоциации аритмологов (EHRA) им могут быть назначены НПОАК при наличии ФП . Единственным исключением считают имплантацию биопротеза пациенту с митральным стенозом. В таких случаях после операции обычно сохраняется выраженная дилатация левого предсердия, что может быть доводом в пользу применения антагониста витамина К.
Присвоение группы инвалидности после стентирования
Возможность получения инвалидности после реваскуляризации зависит от эффективности процедуры (3):
- отличный эффект – приступы стенокардии отсутствуют, переносимость физических нагрузок хорошая;
- хороший эффект – редкие приступы стенокардии, переносимость физических нагрузок, умеренная;
- удовлетворительный эффект – приступы стенокардии остаются, но только после более интенсивных нагрузок;
- неэффективная – состояние больного не изменилось.
При удовлетворительном эффекте группа инвалидности положена, только людям со значительной выраженностью заболевания, ухудшением качества жизни, невозможностью выполнять свою работу. Неэффективная операция при невозможности полной реваскуляризации миокарда – показания к установлению 2 группы.
Наблюдение за пациентами, получающими НПОАК
Хотя НПОАК могут оказать влияние на стандартные показатели свертывания крови, такие как МНО/протромбиновое время и активированное частичное тромбопластиновое время, их измерение перед началом лечения или для оценки эффективности терапии не имеет смысла и не рекомендуется . При терапии НПОАК измерять исходное МНО целесообразно только в период перехода с варфарина или другого антагониста витамина К на НПОАК. В практическом руководстве Европейской ассоциации аритмологов (EHRA, 2018) содержатся общие рекомендации, которые могут быть использованы при лечении любыми НПОАК . По мнению экспертов, лечение этими препаратами можно начать немедленно, если МНО на фоне приема антагониста витамина К составляет ≤2,0. Пациентам со значением МНО от 2,0 до 2,5 НПОАК также можно назначить в тот же день или (лучше) на следующий день. Если МНО превышает 2,5, то перед назначением НПОАК необходимо повторно измерить этот показатель через 1-3 дня. При оценке возможных сроков снижения МНО следует учитывать его исходную величину и период полувыведения антагониста витамина К (аценокумарол – 8-24 ч, варфарин – 36-48 ч, фенопрокумон – 120-200 ч).
Следует отметить, что в инструкциях по применению НПОАК указано, что эти препараты могут быть назначены вместо варфарина, если МНО составляет ≤3 для ривароксабана, ≤2,5 для эдоксабана и ≤2,0 для апиксабана и дабигатрана.
Все НПОАК частично выводятся почками в неизмененном виде, в большей степени дабигатран (80%) и эдоксабан (50%) и в меньшей – ривароксабан (35%) и апиксабан (27%) , поэтому нарушение функции почек может сопровождаться увеличением концентрации препаратов в крови и усилением их антикоагулянтного действия. В связи с этим пациентам с хронической болезнью почек целесообразно назначать ингибиторы фактора Ха, которые в меньшей степени выводятся почками (ривароксабан или апиксабан). При лечении НПОАК необходимо регулярно контролировать функцию почек (по крайней мере ежегодно), чтобы своевременно скорректировать дозу препарата. Например, рекомендуемая доза ривароксабана у пациентов со сниженным клиренсом креатинина (30-50 мл/мин) составляет 15 мг один раз в день. Чтобы определить минимальную кратность определения функции почек (в месяцах) у пациентов с клиренсом креатинина 30-60 мл/мин, его значение следует разделить на 10. Например, если клиренс креатинина составляет 40 мл/мин, то функцию почек необходимо контролировать каждые 4 мес. При наличии дополнительных факторов риска (пожилой возраст, сопутствующие заболевания) может потребоваться более частое мониторирование функции почек, особенно при лечении дабигатраном.